La empresa alemana BioNTech se asoció con Pfizer para desarrollar y probar una vacuna contra la COVID-19 conocida como BNT162b2, con el nombre genérico tozinameran o la marca comercial Comirnaty. Un ensayo clínico demostró que la vacuna tiene una tasa de eficacia del 95 por ciento para la prevención de la enfermedad.
Un fragmento del coronavirus
El virus SARS-CoV-2 está colmado de proteínas que usa para entrar en las células humanas. Estas proteínas, llamadas de espiga, son un blanco tentador para posibles vacunas y tratamientos.

Gen de
proteína de
la espiga

Gen de
proteína de
la espiga
Al igual que la vacuna de Moderna, la de Pfizer-BioNTech se basa en las instrucciones genéticas del virus para armar la proteína de espiga.
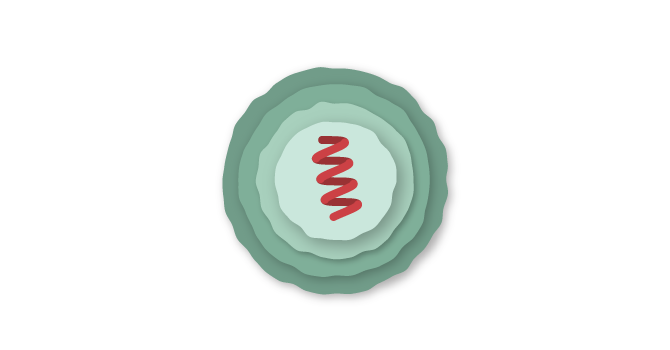
ARNm dentro de una envoltura aceitosa
La vacuna usa ARN mensajero, el material genético que nuestras células leen para producir proteínas. La molécula —abreviada como ARNm— es frágil y nuestras enzimas naturales la harían pedazos si se inyectase directamente en el cuerpo. Para proteger la vacuna, Pfizer y BioNTech envuelven el ARNm en burbujas aceitosas hechas de nanopartículas de lípidos.

Nanopartículas
de lípidos
rodean
el ARNm

Nanopartículas
de lípidos rodean
el ARNm
Debido a su fragilidad, las moléculas de ARNm se desbaratan rápidamente a temperatura ambiente. Pfizer está construyendo contenedores especiales con hielo seco, sensores térmicos y rastreadores GPS para garantizar que las vacunas puedan transportarse a -70 grados Celsius a fin de que sigan siendo viables.
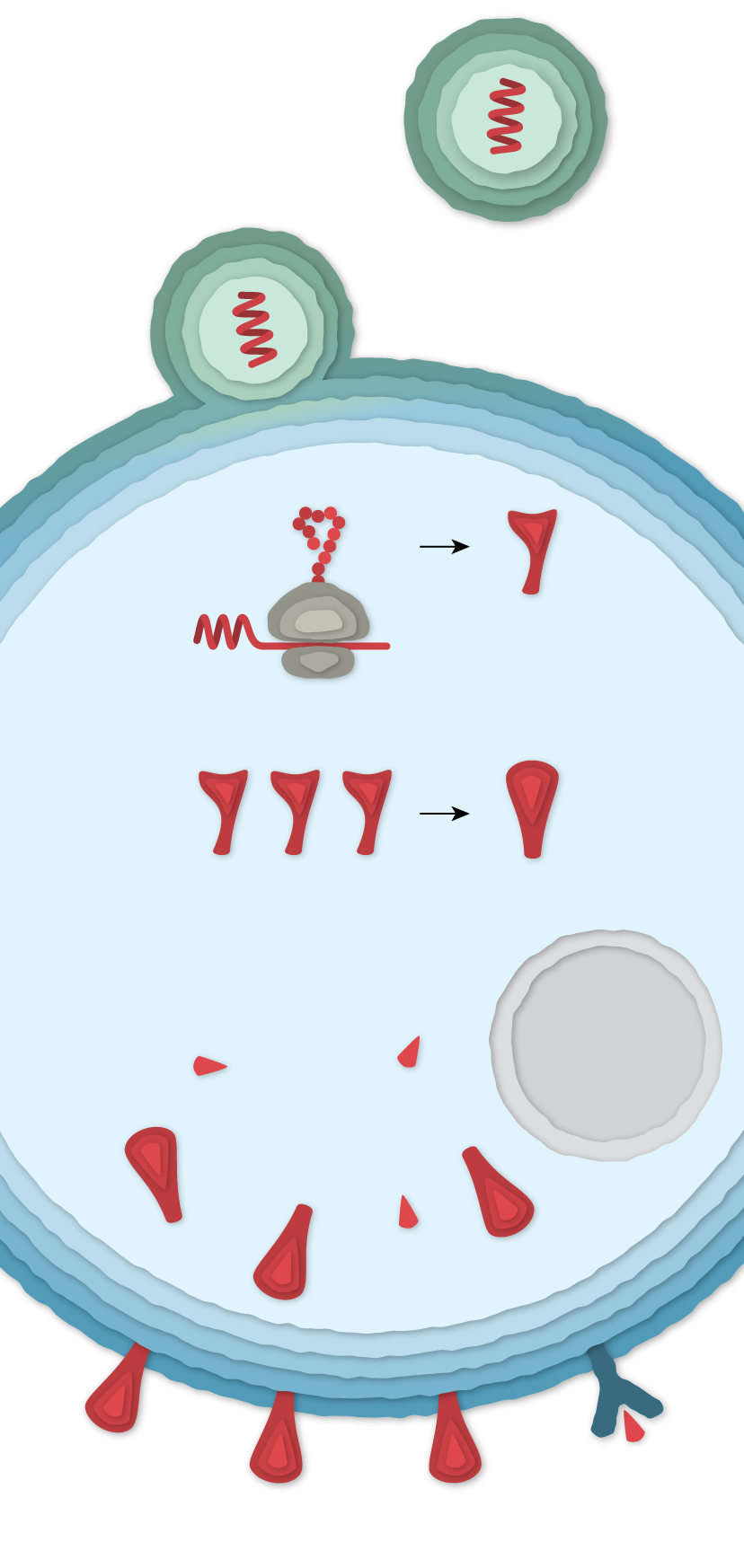
Entrada a una célula
Tras la inyección, las partículas de la vacuna chocan con las células, se fusionan con ellas y liberan el ARNm. Las moléculas de la célula leen su secuencia y ensamblan proteínas de espiga. Al final, la célula destruye el ARNm de la vacuna, por lo que no queda ningún rastro permanente.

Tres proteínas de
espiga se combinan
Fragmentos
de espigas
y proteínas
Presenta
fragmentos
de espiga

Tres proteínas de
espiga se combinan
Fragmentos
de espigas
y proteínas
Presenta
fragmentos
de espiga

Tres proteínas de
espiga se combinan
Fragmentos
de espigas
y proteínas
Presenta
fragmentos
de espiga

Tres proteínas de
espiga se combinan
Fragmentos
de espigas
y proteínas
Presenta
fragmentos
de espiga

Tres proteínas de
espiga se combinan
Fragmentos
de espigas
y proteínas
Presenta
fragmentos
de espiga

Tres proteínas de
espiga se combinan
Fragmentos
de espigas
y proteínas
Presenta
fragmentos
de espiga

Tres proteínas de
espiga se combinan
Fragmentos
de espigas
y proteínas
Presenta
fragmentos
de espiga
Algunas de las proteínas de espiga forman espigas que migran a la superficie de la célula y extienden sus puntas. Las células vacunadas también separan algunas de las proteínas en fragmentos que presentan en su superficie. Entonces, el sistema inmunitario puede reconocer estas espigas protuberantes y fragmentos de proteínas de espiga.
Detección del intruso
Cuando una célula vacunada muere, sus restos contienen muchas proteínas de espiga y fragmentos de proteínas que después puede recoger un tipo de célula inmunitaria llamada célula presentadora de antígenos.

Restos de una
célula muerta
CÉLULA
PRESENTADORA
DE ANTÍGENOS
Digestión de
las proteínas
Presenta
un fragmento de
proteína de espiga

Restos de una
célula muerta
CÉLULA
PRESENTADORA
DE ANTÍGENOS
Digestión de
las proteínas
Presenta
un fragmento de
proteína de espiga

Restos de una
célula muerta
CÉLULA
PRESENTADORA
DE ANTÍGENOS
Digestión de
las proteínas
Presenta
un fragmento de
proteína de espiga
La célula presenta fragmentos de la proteína espiga en su superficie. Cuando otras células llamadas linfocitos T colaboradores detectan estos fragmentos, los linfocitos T colaboradores pueden hacer sonar la alarma y ayudar a convocar a otras células inmunitarias para combatir la infección.
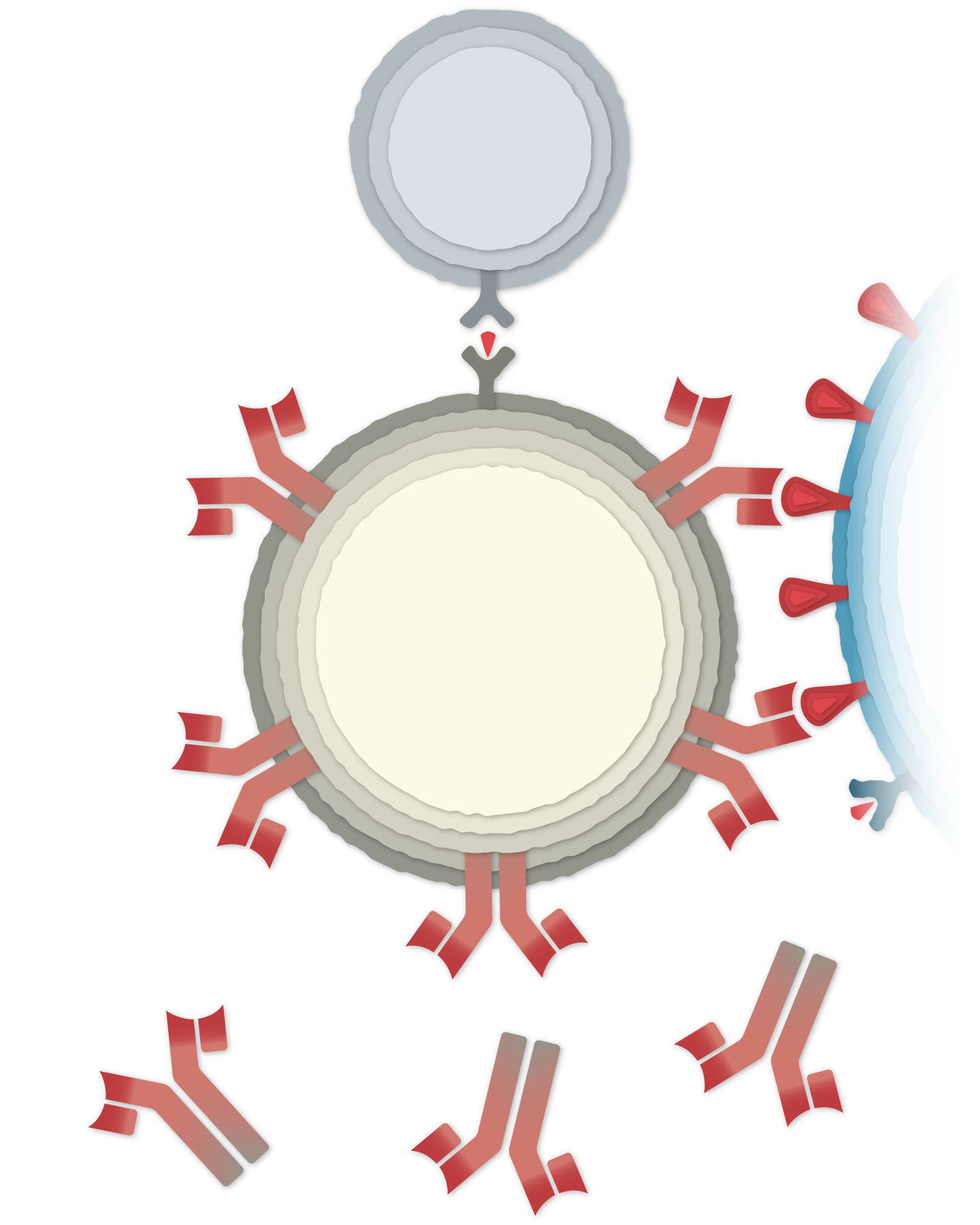
Creación de anticuerpos
Otras células inmunitarias, llamadas linfocitos B, podrían chocar con las espigas del coronavirus en la superficie de las células vacunadas, o con fragmentos de proteínas de espiga que están flotando. Unos cuantos linfocitos B quizá logren adherirse a las proteínas de espiga. Después, si los linfocitos T colaboradores activan estos linfocitos B, comenzarán a proliferar y secretar anticuerpos que atacarán a la proteína espiga.

Proteínas
correspondientes
en la superficie
Activación del
linfocito B

Proteínas
correspondientes
en la superficie
Activación del
linfocito B
Proteínas
correspondientes
en la superficie
Activación del
linfocito B

Proteínas
correspondientes
en la superficie
Activación del
linfocito B

Proteínas
correspondientes
en la superficie
Activación del
linfocito B

Proteínas
correspondientes
en la superficie
Activación del
linfocito B

Activación del
linfocito B
Proteínas
correspondientes
en la superficie

Activación del
linfocito B
Proteínas
correspondientes
en la superficie

Activación del
linfocito B
Proteínas
correspondientes
en la superficie

Activación del
linfocito B
Proteínas correspondientes
en la superficie

Activación del
linfocito B
Proteínas correspondientes
en la superficie

Activación del
linfocito B
Proteínas correspondientes
en la superficie
Virus freno al
Los equipos pueden adherirse a las espigas del coronavirus, marcar el virus para que sea destruido y bloquear la infección al impedir que las espigas se adhieran a otras células.
Supresión de células infectadas
Las células presentadoras de antígenos también pueden activar otro tipo de célula inmunitaria llamada linfocito T citotóxico (o supresor) para que busque y destruya cualquier célula infectada de coronavirus que presente fragmentos de proteína de espiga en su superficie.

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada

CÉLULA
PRESENTADORA
DE ANTÍGENOS
Presentación de
un fragmento de
proteína de espiga
LINFOCITO T
ASESINO
ACTIVADO
Comienza a suprimir
a la célula infectada
Recuerdo del virus
La vacuna de Pfizer-BioNTech requiere dos inyecciones, administradas con 21 días de diferencia, a fin de preparar el sistema inmunitario lo mejor posible para combatir el coronavirus. Sin embargo, ya que la vacuna es nueva, los investigadores no saben cuánto tiempo podría durar su protección.

Segunda dosis
21 días después

Segunda dosis
21 días después

Segunda dosis
21 días después
Un estudio preliminar que la vacuna parece ofrecer una protección sólida unos diez días después de la primera dosis, en comparación con las personas que tomaron un placebo:

Incidencia acumulativa de la COVID-19
entre participantes del ensayo clínico
Gente que tomó
un placebo
Gente que se aplicó la
vacuna de Pfizer-BioNTech
Semanas después de la primera dosis

Incidencia acumulativa de la COVID-19
entre participantes del ensayo clínico
Gente que tomó
un placebo
Gente que se aplicó
la vacuna de
Pfizer-BioNTech
Semanas después de la primera dosis
Es posible que, en los meses posteriores a la inoculación, la cantidad de anticuerpos y linfocitos T citotóxicos disminuya. No obstante, el sistema inmunitario también contiene células especiales llamadas células B y T de memoria que podrían retener información sobre el coronavirus durante años o incluso décadas.
Para más información sobre la vacuna, véase: La vacuna de Pfizer contra la covid: 11 cosas que tienes que saber.
Preparación e inyección
Cada vial de la vacuna contiene 5 dosis de 0,3 mililitros. La vacuna debe descongelarse antes de inocularse y diluirse con solución salina. El vial debe utilizar dentro de las seis horas posteriores a la disolución.
Un vial diluido de la vacuna en el Royal Free Hospital de LondresJack Hill / Agence France-Presse
Fuentes: Centro Nacional de Información de Biotecnología; Naturaleza; Florian Krammer, Escuela de Medicina Icahn en Mount Sinai.