[ad_1]
El domingo, la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) aprobó de emergencia el uso ampliado de plasma sanguíneo rico en anticuerpos para ayudar a los pacientes hospitalizados con coronavirus, lo que permite al presidente Trump, que ha estado presionando a la agencia para que se mueva más rápido para abordar la pandemia, reclamar avances en vísperas de la convención republicana.
Trump citó la aprobación, que se había retrasado por las preocupaciones de los principales científicos del gobierno sobre los datos que la respaldan, como una buena noticia en la lucha contra una enfermedad que ha provocado 176.000 muertes en Estados Unidos y ha dejado a la nación muy por detrás de la mayoría de las demás. en la efectividad de su respuesta.
En una rueda de prensa, describió el tratamiento como “una terapia poderosa” que se hizo posible “al reunir todo el poder del gobierno federal”.
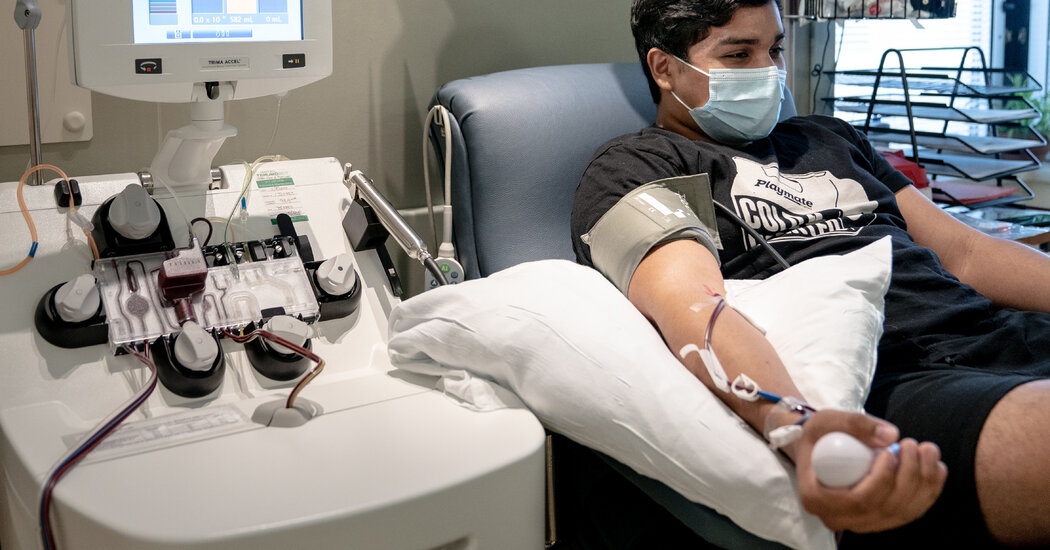
La decisión ampliará el uso de un tratamiento que ya se ha administrado a más de 70.000 pacientes. Pero la F.D.A. citó beneficios solo para algunos pacientes. Y, a diferencia de un nuevo fármaco, el plasma no se puede fabricar en millones de dosis; su disponibilidad está limitada por donaciones de sangre. Trump instó a todos los que se hayan recuperado del virus a donar plasma y dijo que hay una campaña nacional para recolectarlo.
Trump ha presentado sus demandas de reducir la burocracia y acelerar la aprobación de tratamientos y vacunas como una respuesta necesaria a una emergencia de salud pública.
Pero el anuncio del domingo se produjo un día después de que él repitió su afirmación infundada que la F.D.A. estaba retrasando deliberadamente la toma de decisiones hasta después de las elecciones, esta vez citando un “estado profundo”. Esa acusación exacerbó las preocupaciones entre algunos científicos del gobierno, expertos externos y demócratas de que las necesidades políticas del presidente podrían socavar la integridad del proceso regulatorio, dañar la confianza pública en la seguridad e introducir un tipo diferente de riesgo para la salud pública.
Ningún ensayo aleatorizado del tipo que los investigadores consideran más sólido ha mostrado beneficios del plasma de convalecencia. Pero la F.D.A. dijo que los datos que tenía hasta el momento, incluidos más de una docena de estudios publicados, mostraban que “es razonable creer” que el tratamiento “puede ser eficaz para disminuir la gravedad o acortar la duración de la enfermedad Covid-19 en algunos pacientes hospitalizados”. ”En particular aquellos que lo reciben temprano.
Los pacientes menores de 80 años que recibieron plasma con un alto nivel de anticuerpos que combaten el virus dentro de los tres días posteriores al diagnóstico, y que no estaban conectados a un respirador, tenían aproximadamente un 35 por ciento más de probabilidades de estar vivos un mes después en comparación con los que recibieron plasma. con un nivel bajo de anticuerpos, según el Dr. Peter Marks, director del centro de biológicos, evaluación e investigación de la FDA.
Trump eliminó el lenguaje matizado de la agencia durante su comparecencia ante los reporteros en la Casa Blanca, diciendo que se ha demostrado que el plasma convaleciente “reduce la mortalidad en un 35 por ciento”.
La FDA, que es responsable de aprobar nuevos medicamentos, retrasó la autorización durante aproximadamente una semana después de que los principales funcionarios de salud, incluido el Dr. Francis S. Collins, director de los Institutos Nacionales de Salud, y el Dr. Anthony S. Fauci, el principal especialista en enfermedades infecciosas, cuestionó si los datos eran suficientes.
Trump se quejó en un tuit el sábado, alegando sin ninguna evidencia que los funcionarios “esperaban retrasar la respuesta hasta después del 3 de noviembre”, el día de las elecciones, e instando a la F.D.A. para “centrarse en la velocidad y salvar vidas”
Mark Meadows, el jefe de gabinete de la Casa Blanca, también acusó a los reguladores del gobierno durante el fin de semana de demorar la aprobación, calificándola de “un error”. Meadows dijo que Trump no estaba tratando de “tomar atajos”, pero que tenía “una verdadera frustración con algunos de los burócratas que piensan que pueden hacer esto de la manera que normalmente lo hacen”.
En su conferencia de prensa, Trump dio una nota más positiva al decir que la agencia había “realmente mejorado”, especialmente “en los últimos días”.
Los demócratas y algunos expertos en salud dijeron que las críticas del presidente a los reguladores federales socavaron la confianza pública y amenazaron la credibilidad de la agencia encargada de determinar si los medicamentos son seguros y eficaces.
Nancy Pelosi, la presidenta de la Cámara de Representantes, calificó el tuit del sábado de Trump como “muy peligroso”.
Los funcionarios de la Casa Blanca han estado pidiendo una rápida aprobación no solo de los tratamientos de Covid-19, sino también de las vacunas. Sus declaraciones públicas de que una vacuna segura y eficaz podría estar a la vuelta de la esquina han alarmado a los científicos que temen que la presión de la Casa Blanca resulte en una aprobación prematura programada para aumentar las posibilidades de reelección del presidente.
En una reunión del 30 de julio con Pelosi y el senador Chuck Schumer de Nueva York, el líder de la minoría demócrata, altos funcionarios de la administración sugirieron que la administración podría otorgar una aprobación de emergencia para una vacuna antes de que se completen los ensayos de Fase 3 en los Estados Unidos, tal vez tan pronto como Septiembre, según dos personas informadas sobre la discusión. Tal movimiento sería muy inusual y probablemente suscitaría una mayor preocupación sobre si la administración estaba presionando a la F.D.A. aprobar drogas con fines políticos.
Durante la discusión en la sala de conferencias de Pelosi, las personas informadas dijeron que el Sr. Meadows indicó que una vacuna que estaban desarrollando AstraZeneca y la Universidad de Oxford era el candidato más probable para una aprobación temprana. Su discusión fue reportada por primera vez por The Financial Times.
AstraZeneca está llevando a cabo ensayos de Fase 3 en Gran Bretaña, Sudáfrica y Brasil, pero solo comenzó su ensayo clínico de Fase 3 en los Estados Unidos hace unos días.
Los altos funcionarios de la administración cuestionaron el relato de la reunión, diciendo que Meadows y el secretario del Tesoro, Steven Mnuchin, estaban siendo citados erróneamente o habían sido malinterpretados en todos los puntos importantes.
El brote de coronavirus >
Preguntas frecuentes
Actualizado el 17 de agosto de 2020
-
¿Por qué ayuda estar a dos metros de los demás?
- El coronavirus se transmite principalmente a través de gotitas de la boca y la nariz, especialmente cuando tose o estornuda. El C.D.C., una de las organizaciones que usa esa medida, basa su recomendación de seis pies en la idea de que la mayoría de las gotas grandes que las personas expulsan cuando tosen o estornudan caerán al suelo dentro de los seis pies. Pero seis pies nunca ha sido un número mágico que garantice una protección completa. Los estornudos, por ejemplo, pueden lanzar gotas a más de dos metros, según un estudio reciente. Es una regla general: lo más seguro es estar parado a seis pies de distancia afuera, especialmente cuando hace viento. Pero mantén una máscara puesta en todo momento, incluso cuando creas que estás lo suficientemente lejos.
-
Tengo anticuerpos. ¿Soy ahora inmune?
- A partir de ahora, eso parece probable, durante al menos varios meses. Ha habido relatos aterradores de personas que han sufrido lo que parece ser un segundo episodio de Covid-19. Pero los expertos dicen que estos pacientes pueden tener un curso prolongado de infección, y el virus se cobra un número lento de semanas a meses después de la exposición inicial. Las personas infectadas con el coronavirus suelen producir moléculas inmunitarias llamadas anticuerpos, que son proteínas protectoras que se producen en respuesta a una infección. Estos anticuerpos pueden durar en el cuerpo solo de dos a tres meses, lo que puede parecer preocupante, pero eso es perfectamente normal después de que cede una infección aguda, dijo el Dr. Michael Mina, inmunólogo de la Universidad de Harvard. Puede ser posible contraer el coronavirus nuevamente, pero es muy poco probable que sea posible en un corto período de tiempo desde la infección inicial o que las personas se enfermen más la segunda vez.
-
Soy propietario de una pequeña empresa. ¿Puedo obtener alivio?
- Los proyectos de ley de estímulo promulgados en marzo ofrecen ayuda a millones de pequeñas empresas estadounidenses. Los elegibles para la ayuda son empresas y organizaciones sin fines de lucro con menos de 500 trabajadores, incluidas empresas unipersonales, contratistas independientes y autónomos. Algunas empresas más grandes de algunas industrias también son elegibles. La ayuda que se ofrece, que está siendo administrada por la Administración de Pequeñas Empresas, incluye el Programa de Protección de Cheques de Pago y el Programa de Préstamos por Daños Económicos por Desastre. Pero mucha gente aún no ha visto los pagos. Incluso aquellos que han recibido ayuda están confundidos: las reglas son draconianas y algunos están estancados con dinero que no saben cómo usar. Muchos propietarios de pequeñas empresas obtienen menos de lo que esperaban o no escuchan nada en absoluto.
-
¿Cuáles son mis derechos si me preocupa volver a trabajar?
-
¿Cómo será la escuela en septiembre?
- Es poco probable que muchas escuelas vuelvan a un horario normal este otoño, lo que requiere la rutina del aprendizaje en línea, el cuidado infantil improvisado y los días de trabajo atrofiados para continuar. Los dos distritos escolares públicos más grandes de California, Los Ángeles y San Diego, dijeron el 13 de julio que la instrucción será remota en el otoño, citando preocupaciones de que las crecientes infecciones por coronavirus en sus áreas representan un riesgo demasiado grave para los estudiantes y maestros. Juntos, los dos distritos matriculan a unos 825.000 estudiantes. Son los más grandes del país hasta ahora en abandonar los planes de un regreso físico incluso parcial a las aulas cuando vuelvan a abrir en agosto. Para otros distritos, la solución no será un enfoque de todo o nada. Muchos sistemas, incluido el más grande del país, la ciudad de Nueva York, están ideando planes híbridos que implican pasar algunos días en las aulas y otros días en línea. Todavía no existe una política nacional al respecto, así que consulte con su sistema escolar municipal con regularidad para ver qué está sucediendo en su comunidad.
No obstante, sus comentarios sugirieron al menos a algunos participantes que la administración esperaba que los resultados sólidos de los ensayos en el extranjero de AstraZeneca condujeran a una autorización de emergencia temprana, utilizando la misma autoridad que la F.D.A. utilizado para dar luz verde al uso de plasma de convalecencia. Una asistente de Pelosi dijo que advirtió a los funcionarios en la reunión que no tomen atajos.
La F.D.A. generalmente requiere ensayos clínicos con pacientes estadounidenses antes de aprobar vacunas para su uso en este país. Aunque ha habido excepciones a esa regla, dijeron los expertos, la aprobación de una vacuna contra el coronavirus sobre la base de ensayos en el extranjero presentaría problemas desafiantes para los reguladores, en parte debido a las diferencias demográficas y al tamaño de los ensayos.
Un alto funcionario de la administración al que se informó sobre la reunión, que se negó a hablar oficialmente sobre la discusión, dijo que ni Meadows ni Mnuchin sugirieron que se podría aprobar una vacuna a fines de septiembre. El funcionario dijo que la administración no aprobaría una vacuna únicamente sobre la base de ensayos clínicos en el extranjero.
Los portavoces de Meadows y Mnuchin dijeron que ninguno de los dos habló sobre AstraZeneca.
El domingo, Trump volvió a despertar las esperanzas de una vacuna exitosa y dijo: “Te enterarás” de eso “muy pronto, muy pronto”. Dr. Collins, el N.I.H. director, ha dicho que “sería asombroso” si una vacuna estuviera lista para su aprobación en octubre, y que incluso noviembre o diciembre son muy optimistas.
La decisión de la Casa Blanca de aumentar públicamente la presión sobre la F.D.A. inyectó un elemento político en lo que algunos científicos llamaron un avance notable en la expansión del uso de plasma convaleciente. Otros expertos dieron una nota de cautela, diciendo que la evidencia aún era preliminar.
En un comunicado, el presidente de la Sociedad de Enfermedades Infecciosas de América, el Dr. Thomas M. File Jr., dijo que los datos sobre el tratamiento muestran “algunas señales positivas”, pero que “carecemos de los datos de ensayos controlados aleatorios que necesitamos para comprender mejor su utilidad en el tratamiento de Covid-19 “.
En una llamada telefónica con los periodistas el domingo, el Dr. Stephen Hahn, comisionado de la F.D.A., dijo que la agencia continuaría trabajando con los investigadores que estudian el tratamiento y que podría actualizar la autorización. Alentó la continuación de los ensayos aleatorizados para demostrar la eficacia del tratamiento.
“Este no es el final”, dijo.
El Dr. Hahn suavizó la afirmación del presidente de que el tratamiento reduce la mortalidad en un 35 por ciento, diciendo que será cierto “si los datos continúan teniendo éxito”. No quedó claro de inmediato de dónde procedía la cifra del 35 por ciento; no parecía estar incluido en los documentos técnicos publicados por la agencia en apoyo de la decisión.
El Dr. Marks dijo a los periodistas que más de 70.000 pacientes ya habían recibido plasma de convalecencia bajo un programa de agencia especial. La decisión de autorizar el tratamiento para que incluso más médicos pudieran usarlo se basó en un análisis de meses de datos que sugirieron que cuando se administra al comienzo de la enfermedad, el plasma “puede mejorar los resultados y disminuir la mortalidad”, dijo.
“Confiamos en que el plasma convaleciente es seguro de usar en este entorno”, dijo, después de revisar los resultados de los primeros 20.000 pacientes que lo recibieron.
El Dr. Hahn dijo que la decisión de autorizar el tratamiento se tomó “únicamente sobre la base de la ciencia y los datos y nada más”.
Katie Rogers, Nicholas Fandos, Andrew Jacobs y Carl Zimmer contribuyeron con los informes.
[ad_2]
Fuente